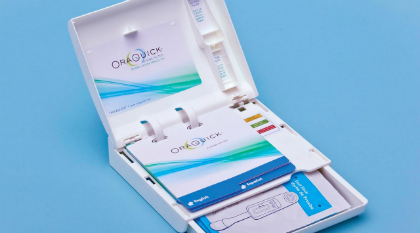
De acordo com a Associated Press, cerca de 240 mil pessoas nos Estados Unidos não sabem que estão infetadas, uma média de uma em cada cinco. Este teste pode, agora, alterar a situação, proporcionando um exame rápido e indolor.
Karen Midthunm, diretora do Centro de Evolução Biológica e Investigação do FDA, afirma que um teste nestes moldes pode ser uma mais-valia, conduzindo mais cedo as pessoas infetadas para o acompanhamento médico apropriado.
Os dados indicam que o OraQuick deverá começar a ser vendido em Outubro, nos Estados Unidos, tanto online como em superfícies comerciais, sendo que o preço do produto ainda não foi definido.
As informações da FDA, entidade responsável pela regulação dos alimentos e dos medicamentos nos EUA, revelam, porém, que o teste não é 100% conclusivo. Nos testes realizados antes da aprovação, foi verificada alguma margem de erro de 8%. Significa isto que houve um teste negativo em cada 12 realizados em indivíduos infetados.
Perante os dados, a instituição aconselha as pessoas cujo resultado do teste tenha sido negativo a realizarem-no, de novo, três meses depois, uma vez que os anticorpos do HIV podem passar despercebidos durante algumas semanas.
Embora a FDA tenha já aprovado, anteriormente, outros testes caseiros de HIV, este é o primeiro que não obriga a um exame sanguíneo nem posterior análise em laboratório. Assim sendo, o novo dispositivo vem assinalar um importante passo na expansão dos testes deste vírus.
[Notícia sugerida por Diana Rodrigues, Maria Manuela Mendes, Sofia Baptista e Patrícia Guedes]